Test o diagnóstico genético preimplantacional (DGP/PGT)
Detecta y evita en el embrión la transmisión de enfermedades graves causadas por alteraciones genéticas y/o cromosómicas, que a veces impiden el embarazo o provocan un aborto temprano o el nacimiento de un niño afecto.
¿Qué es y por qué es importante el DGP?
El Diagnóstico Genético Preimplantacional (DGP) o Test Genético Preimplantacional (PGT), es el análisis de la genética del embrión mediante el estudio de una biopsia de sus células antes de su transferencia al útero materno. Ese conocimiento, nos permite:
- Evitar la transferencia de embriones que por sus anomalías cromosómicas provocarían un aborto temprano o no darían lugar a un bebé sano.
- Localizar y prevenir en la fase de embrión las enfermedades graves causadas por alteraciones genéticas. Logrando asegurar una descendencia sana y acabar con la transmisión de la enfermedad a futuras generaciones.
¿Qué son las alteraciones cromosómicas y monogénicas?
El ser humano nace con 46 cromosomas, 23 de nuestro padre y 23 de nuestra madre que transmitirán nuestra herencia. Contamos con 22 autosomas y un par son cromosomas sexuales, que indicarán el sexo (XX en el caso de las mujeres y XY en el de los hombres). Cada cromosoma es un “gran libro” que contiene las piezas de la información genética que indican cómo son y cómo deben funcionar las células del organismo.
Pero a veces, se producen errores en la división celular que pueden dar lugar a células con demasiadas copias de un cromosoma o, por el contrario, ser insuficientes. Estas anomalías cromosómicas pueden ser:
- numéricas, hay cromosomas de más o de menos;
- estructurales, a un cromosoma le falta o le sobra una parte, está en otro cromosoma o se encuentra invertido.
La anomalía en el número y disposición de los cromosomas del embrión, es la causa más frecuente de fallo implantatorio y el aborto precoz y además se ve incrementada con la edad materna. Por eso el PGT-A de aneuploidías es una herramienta muy útil tanto de diagnóstico, como de tratamiento, en nuestra Unidad de fallo de implantación embrionario.
Otras veces la alteración se produce en un gen concreto que afecta al funcionamiento del organismo provocando una enfermedad monogénica, que es el grupo de enfermedades que se pueden transmitir a la descendencia.
Tipos de diagnóstico genético preimplantacional
- PGT-A anomalías cromosómicas. El test genético preimplantacional para detectar aneuploidías.
- PGT-A Advanced. Además de aneuploidías, permite detectar triploidías y haploidías.
- PGT-M monogénicas. El test genético preimplantacional para detectar enfermedades monogénicas.
- PGT-SR. Que diagnostica alteraciones estructurales.
- PGT-SR Advanced. Una mejora del PGT-SR que permite seleccionar los embriones que detienen la transmisión familiar de la alteración.
A continuación, se describen con detalle:
1. PGT-A el test genético preimplantacional para el análisis de aneuploidías (anomalías cromosómicas)
| Las alteraciones cromosómicas en los embriones son una de las principales causas de la baja tasa de embarazo. Solo los embriones con un número exacto de cromosomas permiten el nacimiento de un bebe sano. Esta técnica permite descartar los embriones alterados, a pesar de que por su aspecto resulten de buena calidad.
Evitando su transferencia se remedia que la pareja se enfrente a la gestación de un bebé afectado; que el embrión no implante o que se produzca un aborto temprano. Por ejemplo, una copia de más en el cromosoma 21 sería la causa del origen del síndrome de Down (trisomía 21). Otras aneuploidías cromosómicas (un cromosoma de más o de menos) comunes son la trisomía 18; trisomía 15; o 47 y el XXY (síndrome de Klinefelter). |
¿A quién se recomienda el PGT-A?
- En los casos de edad materna avanzada, de más de 35 años
- Mujeres que han sufrido abortos de repetición y/o fallos previos de implantación embrionaria en dos o más ciclos de fecundación in vitro.
- Pacientes que tienen diagnosticadas anomalías cromosómicas.
- Parejas en las que se ha identificado un factor masculino severo como causa de la infertilidad.
En qué consiste el PGT-A paso a paso

- En la consulta, el ginecólogo realizará el diseño del tratamiento, que se inicia con la regla.
- Se efectúa la estimulación ovárica para la obtención de los ovocitos.
- En un ciclo de fecundación in vitro FIV obtenemos los embriones.
- Cuando el embrión tiene 5-6 días de desarrollo –fase de blastocisto- extraemos varias células, a través de la técnica de biopsia embrionaria.
- Criopreservamos los embriones hasta el momento de su transferencia.
- Se procesa la biopsia para su análisis cromosómico y obtenemos el diagnóstico.
- Con el resultado se realiza la preparación endometrial de la madre y preparamos la transferencia de un embrión sin alteraciones cromosómicas; descartando los embriones anómalos y evitando transferencias infructuosas.
2. PGT-A Advanced: una mejora del PGT-A que permite seleccionar los embriones que tengan mayor probabilidad de generar un embarazo
| Si el Test Genético Preimplantacional para Aneuploidías (PGT-A) permite descartar los embriones cromosómicamente alterados, el PGT-A Advanced posibilita además conocer el origen específico de estas alteraciones para seleccionar los embriones que tengan mayor probabilidad de generar un embarazo. Este avance proporciona informacional adicional crucial. Por ejemplo, si la alteración cromosómica se originó en el padre o la madre. También, permite detectar triploidías, una condición caracterizada por la presencia de tres juegos de un mismo cromosoma y que podía producir abortos o pruebas de embarazos negativas, y haploidías, en las que hay un solo juego de cromosomas. |
¿A quién se recomienda el PGT-A Advanced?
- En los casos de edad materna avanzada, de más de 35 años.
- Mujeres que han sufrido abortos de repetición y/o fallos previos de implantación embrionaria en dos o más ciclos de fecundación in vitro.
- Pacientes que tienen diagnosticadas anomalías cromosómicas.
- Parejas en las que se ha identificado un factor masculino severo como causa de la infertilidad.
- Parejas con mujeres menores de 35 años, con alta tasa de aneuploidías y/o aquellos (independientemente de la edad) con fecundaciones anómalas.
En qué consiste el PGT-A Advanced paso a paso
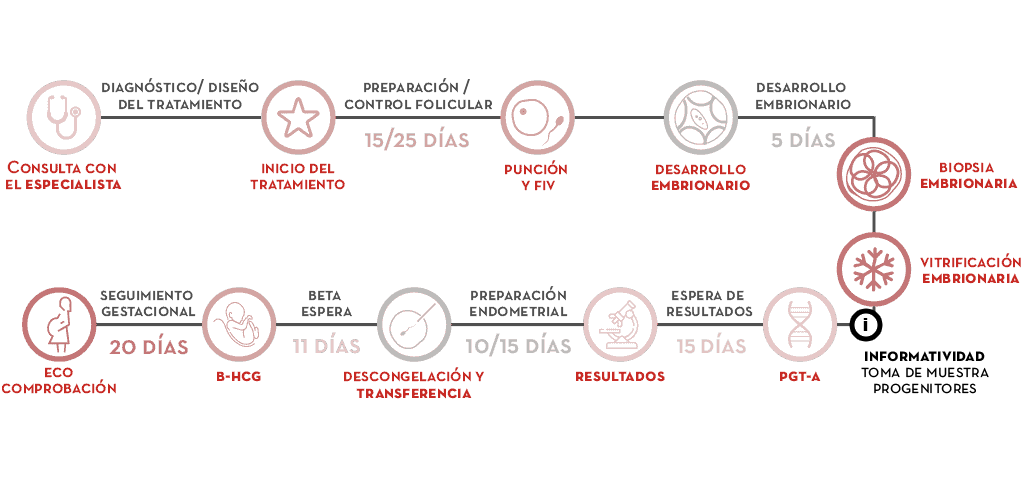
- En la consulta, el ginecólogo realizará el diseño del tratamiento, que se inicia con la regla.
- Se efectúa la estimulación ovárica para la obtención de los ovocitos.
- En un ciclo de fecundación in vitro FIV obtenemos los embriones.
- Cuando el embrión tiene 5 ó 6 días de desarrollo —fase de blastocisto— extraemos varias células, a través de la técnica de biopsia embrionaria.
- Criopreservamos los embriones hasta el momento de su transferencia.
- Se toma una muestra genética de ambos progenitores.
- Se procesa la biopsia para su análisis cromosómico y obtenemos el diagnóstico.
- Con el resultado se realiza la preparación endometrial de la madre y preparamos la transferencia de un embrión sin alteraciones cromosómicas, descartando los embriones anómalos y evitando transferencias infructuosas.
3. PGT-M el test genético preimplantacional para detectar enfermedades monogénicas
| Consiste en el análisis genético de los embriones de una pareja portadora de una enfermedad hereditaria. Permite detectar la alteración o la mutación en un gen que causa la enfermedad. El primer paso es realizar el estudio genético a los futuros padres para identificar el fallo en el gen (mutación) que provoca la enfermedad -estudio genético-.Una vez disponemos del estudio genético el siguiente paso consiste en realizar el estudio de informatividad que permite diseñar una estrategia de diagnóstico específica para esa enfermedad en esa familia. Las afecciones pueden ser autosómicas recesivas, autosómicas dominantes y ligadas al cromosoma X como el síndrome de X frágil, la hemofilia A, la fibrosis quística, la enfermedad de Huntington, la anemia falciforme, la enfermedad de Marfan, etc. |
¿A quién se recomienda el PGT-M?
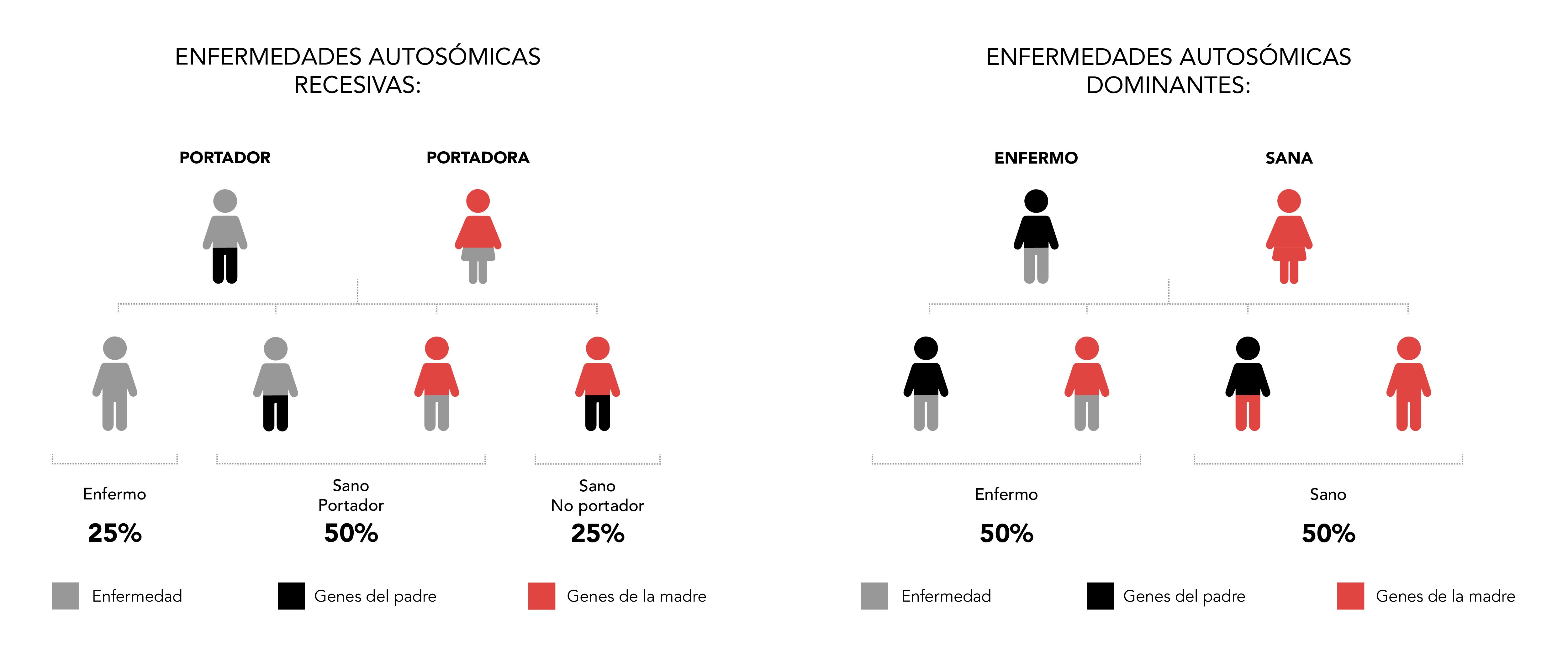
- Parejas en las que uno de los miembros está afectado por una enfermedad genética que se heredaría de forma dominante (el 50% de sus hijos serían enfermos).
- Parejas en las que la madre es portadora de una enfermedad genética ligada al sexo (el 50% sus hijos serán enfermos).
- Parejas en los que ambos miembros de la pareja son portadores de una enfermedad genética que se hereda de forma recesiva (25% de sus hijos serían enfermos).
En qué consiste el PGT-M paso a paso
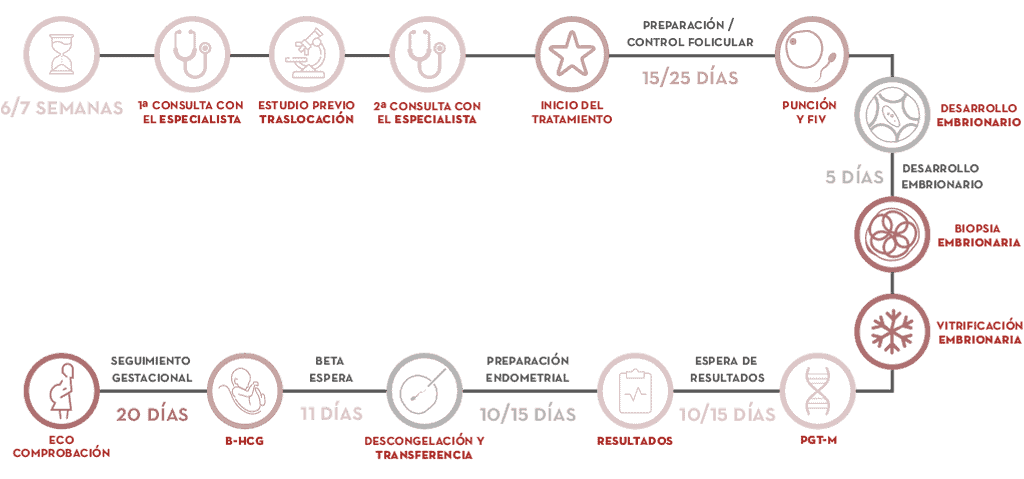
- El primer paso es disponer del estudio genético de los padres. Debemos abordar el caso concreto identificando el fallo en el gen (mutación) que causa la enfermedad.
- A continuación, se realiza el estudio de informatividad, que consiste en desarrollar la estrategia que nos permita identificar la alteración en los embriones. Muchas veces es necesario que participen en el estudio miembros de la familia sanos y afectos.
- Se inicia el ciclo de fecundación in vitro. Una vez que la mujer tiene la regla comienza la estimulación ovárica controlada y entre 15 y 25 días después se realiza la obtención de ovocitos.
- En el laboratorio son fecundados con el semen de la pareja o de donante y se cultivan hasta el día 5-6, embrión en fase de blastocisto, que es el momento en el que se realiza la biopsia embrionaria, consiste en extraer varias células para su análisis genético. Estos embriones se criopreservan a la espera de los resultados.
- Se procesa la biopsia para su análisis genético y obtenemos el diagnóstico.
- Con el resultado se realiza la preparación endometrial de la madre y se prepara la transferencia de un embrión sin alteración del gen estudiado.
4. PGT-SR el test genético preimplantacional para la detección de alteraciones estructurales
| Detecta aquellos embriones que tienen cromosomas anómalos porque están “rotos” o porque hay una unión incorrecta de segmentos. Estas anomalías cromosómicas estructurales son de muchos tipos: delecciones, translocaciones, duplicaciones, inserciones, inversiones y anillaciones. La enfermedad se presenta en los casos en los que el gen no puede expresarse correctamente debido a la alteración que sufre la estructura del cromosoma. |
Tipos de anomalías cromosómicas estructurales
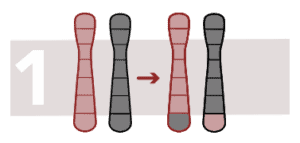
Translocación recíproca equilibrada
La translocación es un tipo de anomalía cromosómica en la que un cromosoma se rompe y una parte se une a un cromosoma distinto. Es recíproca cuando se produce por transferencias de segmentos entre dos cromosomas, cambiando la configuración, pero no el número de cromosomas.
Hablamos de translocación recíproca equilibrada cuando la reorganización no produce pérdida ni ganancia de material cromosómico. Se produce cuando una región cromosómica cambia de posición en el genoma.
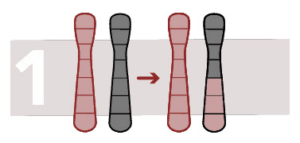
Translocación recíproca desequilibrada
La reorganización provoca una pérdida o una ganancia de material cromosómico. Se produce un cambio en el número de copias en una región cromosómica. Es posible encontrar fragmentos de un cromosoma en otro cromosoma.
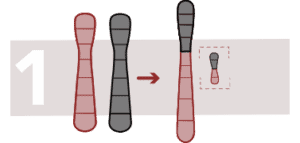
Translocación Robertsoniana
Se produce una fusión de dos cromosomas acrocéntricos (con un solo brazo), se pierden los extremos y los dos cromosomas quedan unidos en uno. Los afectados tienen 45 en lugar de 46 cromosomas y el riesgo de trisomía es mayor.
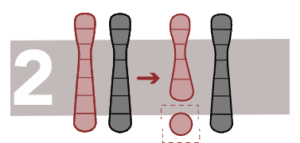
Delecciones
Es la pérdida de un fragmento de ADN de un cromosoma.
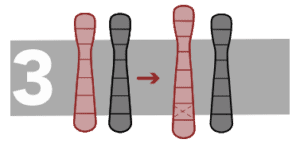
Duplicaciones
Un segmento de un cromosoma se repite a continuación del fragmento original y produce una o más copias de un gen o región de un cromosoma.
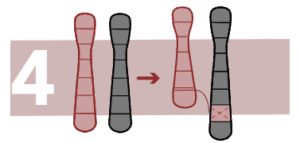
Inserciones
Una parte de un cromosoma se ha insertado en una posición inusual dentro del mismo u otro cromosoma. Si no hay ganancia o pérdida de material cromosómico la persona será sana.
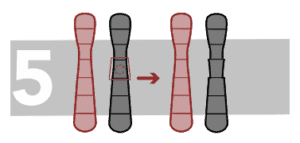
Inversiones Paracéntricas
Hablamos de inversiones cuando una parte del cromosoma se rompe en dos puntos y el segmento interior gira al revés para luego volver a unirse. Las inversiones paracéntricas se producen cuando la inversión no implica al centrómero.
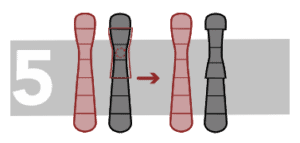
Inversiones Pericéntricas
En este caso el fragmento invertido incluye el centrómero.
Anillaciones
Los extremos de un cromosoma se han roto y se han unido en sus extremos formando un anillo. Provoca enfermedades genéticas y la más frecuente es el síndrome de Turner.
¿A quién se recomienda?
A parejas en las que uno de los miembros es portador de una alteración cromosómica estructural.
En qué consiste el PGT-SR paso a paso
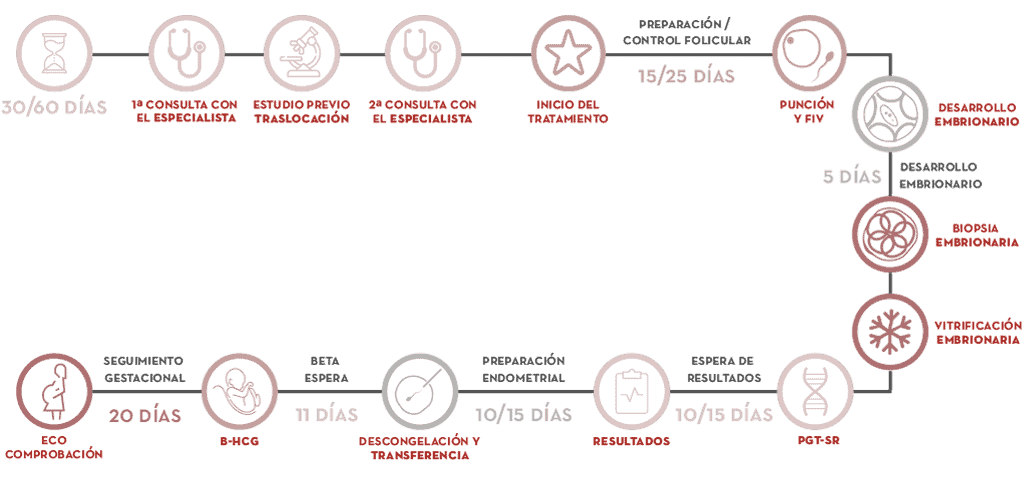
- En la primera consulta el ginecólogo valorará su caso.
- Puede ser necesario el estudio previo de la alteración estructural.
- En la siguiente consulta se realizará el diagnóstico y diseño del tratamiento que comienza con la regla.
- Se efectúa la estimulación ovárica para la obtención de los ovocitos.
- En un ciclo de fecundación in vitro FIV se obtienen los embriones.
- Cuando el embrión tiene 5-6 días de desarrollo –fase de blastocisto- extraemos varias células a través de la técnica de biopsia embrionaria.
- Criopreservamos los embriones hasta el momento de su transferencia.
- Se procesa la biopsia para su análisis cromosómico y obtenemos el diagnóstico.
- Con el resultado se realiza la preparación endometrial de la madre. Preparamos la transferencia de un embrión sin alteraciones cromosómicas; descartando los embriones anómalos y evitando transferencias infructuosas.
4. PGT-SR Advance una mejora del PGT-SR que permite seleccionar los embriones que detienen la transmisión familiar de la alteración
| Si el Test Genético Preimplantacional para alteraciones cromosómicas estructurales (PGT-SR) permite descartar los embriones cromosómicamente desbalanceados. El PGT-SR Advanced, posibilita además identificar si el embrión es portador de la alteración cromosómica balanceada de sus progenitores o posee un cariotipo totalmente normal, evitando que en un futuro el niño nacido tenga que someterse a un PGT-SR para obtener descendencia. Este avance proporciona información adicional crucial ya que detiene la transmisión familiar de la alteración cromosómica. También, permite detectar triploidías, una condición caracterizada por la presencia de tres juegos de un mismo cromosoma y que podía producir abortos o pruebas de embarazos negativas, y haploidías, en las que hay un solo juego de cromosomas. |
¿A quién se recomienda?
A parejas en las que uno de los miembros es portador de una alteración cromosómica estructural.
En qué consiste el PGT-SR Advanced paso a paso
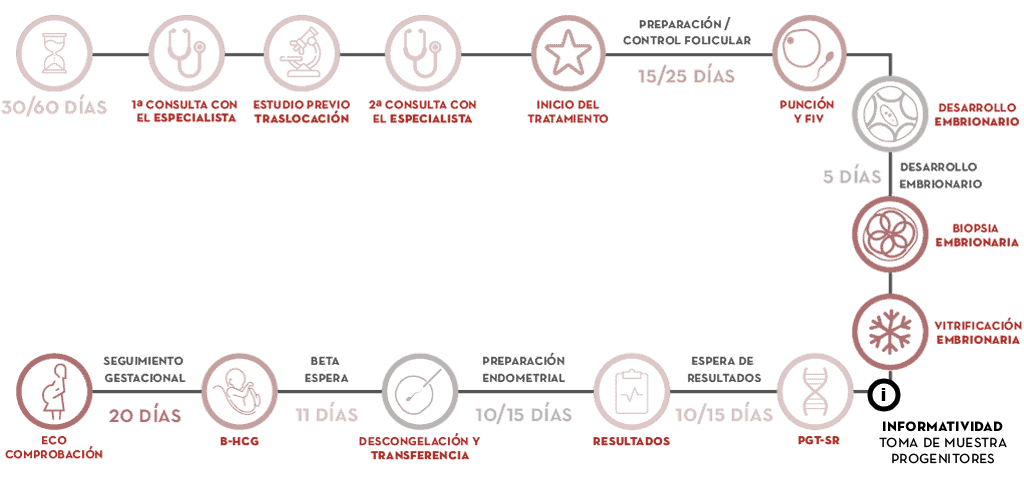
- En la consulta, el ginecólogo realizará el diseño del tratamiento, que se inicia con la regla.
- Se efectúa la estimulación ovárica para la obtención de los ovocitos.
- En un ciclo de fecundación in vitro FIV obtenemos los embriones.
- Cuando el embrión tiene 5 ó 6 días de desarrollo —fase de blastocisto— extraemos varias células, a través de la técnica de biopsia embrionaria.
- Criopreservamos los embriones hasta el momento de su transferencia.
- Se procesa la biopsia para su análisis cromosómico y obtenemos el diagnóstico.
- Se toma una muestra genética de ambos progenitores. En algunos casos es necesario disponer de una muestra de algún familiar portador de la alteración cromosómica estructural.
- Con el resultado se realiza la preparación endometrial de la madre y preparamos la transferencia de un embrión sin alteraciones cromosómicas, descartando los embriones anómalos y evitando transferencias infructuosas. Se priorizará la transferencia de embriones balanceados normales frente a los portadores de la traslocación.

TEST O DIAGNÓSTICO GENÉTICO PREIMPLANTACIONAL (DGP/PGT)
Ventajas de realizar el DGP/PGT
Mejora la selección embrionaria, sabremos cuáles son los embriones que no tienen alterado el número de cromosomas y que darán lugar a un niño sano.
Evita transferir embriones que no implantarán. Hay alteraciones cromosómicas incompatibles con la vida que impiden que el embrión se desarrolle en sus etapas iniciales o que implante en el útero materno.
No se implantarán embriones que causen abortos o nacimientos de niños con distintos síndromes.
Disminuye el tiempo para lograr el embarazo. Evitamos transferir embriones que no darán lugar a un niño sano o van a bloquearse en su desarrollo.
Menor coste. Evitará congelar y transferir embriones que no son sanos genéticamente, aunque por su aspecto lo parezcan, eliminando el coste de la transferencia de estos embriones que sabremos que no serán viables.
Mejora el bienestar psicológico. Garantiza que el embrión es sano y rebaja la posibilidad del riesgo de aborto y con ello la tensión emocional que esto implica en la pareja.
Inconvenientes del DGP/PGT
Es un procedimiento invasivo ya que se debe biopsiar el embrión para realizar la prueba genética.
Ciclo sin transferencia. Se corre el riesgo de que todos los embriones sean cromosómicamente anómalos y no pueda hacerse una transferencia. Ello provoca por un lado la interrupción del tratamiento y por otro un revés emocional.
Mosaicismo embrionario. Gracias a la precisión de las técnicas de análisis genético podemos saber si el embrión tiene células normales y alteradas, conocido como mosaicismo. Está por determinar si esto afecta de alguna forma al embrión. Distintos trabajos de investigación de Instituto Bernabeu van en este sentido.
Método de screening. La biopsia al embrión analiza la parte externa para dejar intacta la parte que dará lugar al bebé. Numerosos trabajos científicos han demostrado un alto grado de correlación entre ambos. Asumimos que la muestra que tomamos es representativa de todo el embrión.
Dificultad para tomar la decisión. A muchas parejas les resulta doloroso tomar la decisión de analizar sus embriones, bien por aspectos éticos o emocionales. Además, cuentan en nuestro centro con asesoramiento genético, psicológicos y profesional para orientarles si así lo desean.