
Tout ce que vous devez savoir sur la vitrification de l’embryon
La vitrification nous permet de préserver les embryons et de les rendre disponibles à l’avenir. Cette technique a été intégrée à la reproduction assistée et a remplacé le reste des techniques de cryoconservation en raison de sa simplicité et de son efficacité.
Índice
- 1 Quelle est la différence entre la congélation, la cryopréservation et la vitrification?
- 2 En quoi consiste la vitrification de l’embryon?
- 3 Quand faut-il vitrifier les embryons?
- 4 Quels sont les avantages de la vitrification de l’embryon?
- 5 Quel est le meilleur moment pour vitrifier les embryons et quels sont les taux de réussite?
- 6 Vitrification: réalisation de la technique et différents supports
- 7 Taux de réussite de la vitrification des embryons
- 8 Combien de temps les embryons peuvent-ils être cryopréservés?
Quelle est la différence entre la congélation, la cryopréservation et la vitrification?
En termes biologiques, on parle de congélation d’une cellule ou d’un embryon, pour les maintenir à basse température dans un état latent de vie suspendue. On paralyse leur activité physiologique pour qu’à l’avenir ils puissent être dégelés et reprendre toutes leurs fonctions.
Lorsque nous amenons ces cellules ou embryons à très basses températures, on parle de cryoconservation.
Il existe plusieurs méthodes de cryoconservation et dans toutes, l’objectif à atteindre est commun: éviter la formation de cristaux de glace, car ceux-ci endommagent la structure de la membrane des cellules, entraînant leur mort ou leur lyse. Les cellules sont principalement constituées d’eau, c’est donc un grand défi à relever. L’une de ces méthodes de cryopréservation est la vitrification.
En quoi consiste la vitrification de l’embryon?
La vitrification est basée sur l’utilisation d’une forte concentration de molécules cryoprotectrices, qui aident à la déshydratation des cellules et, en association avec une baisse rapide de la température, forment un état solide amorphe sans formation de cristaux.
Quand faut-il vitrifier les embryons?
Il existe plusieurs scénarios dans lesquels nous avons un embryon de bonne qualité dans le laboratoire de FIV qui ne va pas être transféré dans l’utérus de la mère à ce moment-là et que nous pouvons vitrifier pour qu’il puisse être transféré à l’avenir. On vitrifiera des embryons dans les scénarios suivants, entre autres:
- Si un transfert d’embryons est effectué et qu’il reste des embryons de bonne qualité.
- Lorsque le transfert est planifié, mais qu’un certain facteur survient et entraîne qu’il est déconseillé de l’effectuer à ce moment. Par exemple, des découvertes inattendues dans l’utérus au moment du transfert, des niveaux d’hormones inadéquats, etc.
- Si, après une stimulation ovarienne, il existe un risque élevé de développer un syndrome d’hyperstimulation ovarienne. Dans ces cas, nous reporterons le transfert au cycle suivant, ce qui éliminera totalement ce risque (transfert différé).
- Si, au moment du transfert, il est impossible d’accéder à la cavité utérine.
- Lorsque nous effectuons une biopsie d’embryon pour un diagnostic génétique préimplantatoire (DPI). Dans ces cas, les embryons biopsiés sont vitrifiés en attendant le diagnostic.
- Dans les traitements de double stimulation, dans lesquels, après une première collecte d’ovocytes, ils sont cryopréservés et une seconde stimulation est initiée quelques jours plus tard. Après la deuxième collecte, les ovocytes de la première stimulation sont dévitrifiés pour augmenter le nombre d’ovocytes disponibles et on procède au traitement de fécondation in vitro dans lequel les embryons sont vitrifiés pour effectuer le transfert dans la phase appropriée du cycle menstruel.
- Dans un traitement de fécondation in vitro avec don d’ovocytes dans lequel il n’est pas possible de synchroniser la préparation de l’utérus de la mère réceptrice avec la stimulation ovarienne de la donneuse. Chez certaines femmes, l’utilisation d’hormones pour la préparation contrôlée de l’utérus est contre-indiquée et elles doivent être transférées au moment adéquat de leur cycle menstruel (transfert de cycle naturel), ce qui rend difficile la synchronisation avec la donneuse. La possibilité de cryopréserver les embryons pour un transfert ultérieur dans un cycle naturel est possible grâce à la vitrification.
- Lorsque des circonstances extérieures au traitement rendent impossible de compléter le traitement par un transfert d’embryons. Un exemple clair est la situation vécue en mars 2020, lorsque l’urgence sanitaire a obligé à paralyser l’activité des laboratoires de fécondation in vitro. Effectivement, les sociétés scientifiques à l’époque ont conseillé d’arrêter les traitements de procréation assistée qui étaient en cours en raison du manque de connaissances sur les effets négatifs de la Covid-19 pendant la grossesse.
Quels sont les avantages de la vitrification de l’embryon?
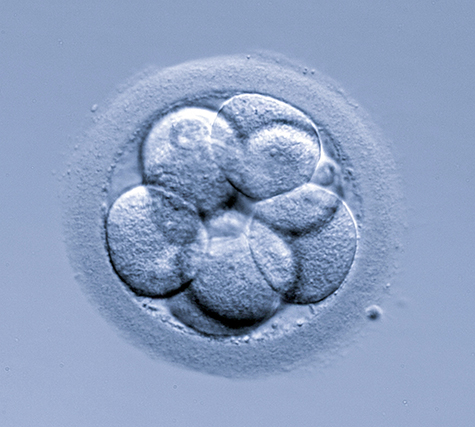
La vitrification de l’embryon offre de grands avantages à la reproduction assistée.
- La première est qu’à partir d’une seule ponction, nous pouvons effectuer plusieurs transferts d’embryons, ce qui augmente les chances de réussite par ponction, c’est-à-dire le taux de grossesse cumulé.
- La vitrification des embryons offre également une sécurité dans les traitements de FIV, car elle permet de reporter les transferts pour éviter des risques tels que l’hyperstimulation ovarienne.
- Comme il existe plusieurs tentatives d’obtention de grossesse par ponction, de plus en plus de personnes choisissent de transférer un seul embryon. La vitrification de l’embryon permet donc de réduire le nombre de grossesses multiples, qui comportent des risques plus importants pour le fœtus et la mère.
- Un autre point fort du transfert d’embryons cryopréservés est la simplicité des traitements hormonaux pour la patiente par rapport à ceux requis pour la stimulation ovarienne. Cela signifie un plus grand confort pour la patiente et un coût beaucoup plus faible en médicaments. Dans certains cas, cela se fait dans ce que nous appelons un « cycle naturel », qui ne nécessite aucun médicament.
- Certaines études ont observé de meilleurs résultats lorsqu’il est transféré dans un cycle postérieur à celui où la stimulation ovarienne est effectuée, qui produit un environnement utérin qui n’est pas considéré comme optimal. Se concentrer sur la préparation de l’utérus pour obtenir les meilleures conditions est également un point favorable à la vitrification de l’embryon.
- Enfin, nous avons vu auparavant que, pour de nombreuses raisons différentes, il n’est parfois pas possible d’effectuer un transfert à frais. Dans ces cas, sans la vitrification, il y aurait des personnes qui ne pourraient pas terminer leurs traitements, donc nous pouvons affirmer que dans ces cas, la vitrification de l’embryon est bien plus qu’un avantage, c’est une porte ouverte, la manière d’obtenir la grossesse désirée.
Quel est le meilleur moment pour vitrifier les embryons et quels sont les taux de réussite?
Il est possible de vitrifier les embryons tous les jours de leur développement en laboratoire, bien que les résultats de la survie et leur potentiel de donner lieu à une grossesse varient selon le jour où ils sont cryopréservés.
Au début de la fécondation in vitro, nous travaillions au stade du zygote (embryon au jour 1, avec une seule cellule) ou dans des embryons en phase de division (jour 2 et jour 3, embryons de 2 à 8 cellules). Cependant, l’amélioration des milieux de culture et des équipements d’incubation nous a permis de développer ce que nous appelons la « culture longue » qui consiste à maintenir les embryons jusqu’au 5ème ou 6ème jour de culture afin qu’ils atteignent le stade de blastocyste (embryon d’environ 200 cellules). Cela nous permet de mieux sélectionner les embryons (puisque nous pouvons écarter ceux qui ne peuvent pas atteindre le stade de blastocyste). En outre, elle améliore théoriquement la synchronisation de l’embryon avec l’utérus, puisque dans une conception in vivo, les embryons n’atteignent pas l’utérus avant ce moment. Un grand avantage de la culture jusqu’au stade de blastocystes est que ces derniers réagissent très bien à la vitrification.
Mais un facteur crucial qui déterminera les chances pour un embryon de survivre à la décongélation et de pouvoir aboutir à une grossesse est la qualité de l’embryon. Il existe plusieurs critères pour classer les embryons. Dans les principaux systèmes de classification, les embryons peuvent être regroupés en quatre catégories: A, B, C et D. Les embryons de type A et de type B sont des embryons de bonne qualité. Les embryons de type C sont des embryons de qualité moyenne à basse et les embryons de type D sont des embryons de mauvaise qualité avec presque aucune chance de grossesse.
Pour résister aux processus de vitrification et de dévitrification, un embryon doit être de bonne qualité. Par conséquent, les critères de classification doivent être appliqués correctement et des embryons de bonne qualité doivent être sélectionnés pour la congélation.
Vitrification: réalisation de la technique et différents supports
De nos jours, il existe des supports commerciaux spécifiques pour la vitrification des ovocytes et des embryons qui ont des protocoles très simples. Les différences entre les différentes sociétés commerciales résident dans les cryoprotecteurs choisis et leur concentration, mais en général le processus est assez similaire pour tous les milieux commerciaux.
Le développement de la technique consiste à faire passer les embryons à travers les différents milieux de vitrification et à les placer finalement dans une petite quantité de milieu sur un support qui sera immergé dans de l’azote liquide.
C’est dans le type de support que nous trouvons des différences. Il existe des dispositifs ouverts, dans lesquels l’embryon entre en contact direct avec l’azote liquide pendant la vitrification. Dans le processus de dévitrification, il entre également en contact avec le milieu de dévitrification, ce qui permet une augmentation très rapide de la température (une étape clé pour la survie de l’embryon). Mais ce contact direct avec l’azote pendant la durée du stockage pose un risque théorique de contamination. L’un des dispositifs ouverts les plus connus est le Cryotop® de Kitazato.
Pour éviter le risque de contamination, il est préférable d’utiliser des dispositifs fermés qui, avec une bonne conception, permettent également ce réchauffement rapide si crucial dans la dévitrification. Parmi les dispositifs de ce type, on trouve les paillettes haute sécurité VHS CBS de Cryo Bio System ou le système fermé Cryotop® de Kitazato.
Taux de réussite de la vitrification des embryons
Lorsqu’un puissant programme de cryoconservation d’embryons est disponible, comme celui développé à l’Instituto Bernabeu, la vitrification offre des taux de survie très élevés, avec une moyenne de 98 %.
Comme on peut le voir, les embryons dévitrifiés ont de très fortes probabilités de revenir à leur état initial après décongélation et offrent de très bonnes probabilités d’aboutir à une grossesse, en fonction bien sûr du cas spécifique de chaque patient.
Combien de temps les embryons peuvent-ils être cryopréservés?
À des températures aussi basses que l’azote liquide (- 196 ºC) dans lequel les embryons sont stockés, aucune réaction chimique ne se produit. Par conséquent, les embryons restent indéfiniment dans un état inchangé.
Fin 2020, la nouvelle de la naissance, en octobre, de la petite Molly dans le Tennessee (États-Unis) s’est répandue dans le monde entier. La petite fille a battu le record de l’embryon le plus longtemps cryopréservé et qui a donné naissance, étant transférée 27 ans après sa cryopréservation. Cela nous donne une idée du potentiel que les techniques de cryoconservation ont dans le domaine de la reproduction assistée.
Mª Carmen Tió, biologiste de l’Instituto Bernabeu
