Test of Preïmplantatie Genetische Diagnostiek (PGD)
Detecteert en voorkomt de overdracht van ernstige aandoeningen in het embryo die worden veroorzaakt door genetische en/of chromosomale afwijkingen die soms een zwangerschap verhinderen of leiden tot een vroege miskraam of de geboorte van een aangetast kind
Wat is PGD en waarom is het belangrijk?
Preïmplantatie Genetische Diagnotiek (PGD) of Preïmplantatie Genetische Test (PGT), is de analyse van de genetica van het embryo door middel van de studie van een biopsie van de cellen voor de terugplaatsing naar de moederlijke baarmoeder. Deze kennis biedt ons de mogelijkheid om:
- Het vermijden van de terugplaatsing van embryo’s die vanwege de chromosomale afwijkingen een vroege miskraam zouden veroorzaken of niet tot een gezonde baby zouden leiden.
- Het lokaliseren en voorkomen van ernstige aandoeningen die worden veroorzaakt door genetische afwijkingen in de embryonale fase. Het verzekeren van een gezond nageslacht en de overdracht van de aandoening op toekomstige generaties voorkomen.
Wat zijn chromosoom- en monogenische afwijkingen?
De mens heeft van geboorte 46 chromosomen, 23 van de vader en 23 van de moeder. Deze geven onze erfenis door. We hebben 22 autosomen en het overige paar zijn geslachtschromosomen die het geslacht (XX voor vrouwen en XY voor mannen) aangeven. Elk chromosoom is een “groot boek” dat stukjes genetische informatie bevat en aangeven hoe de cellen in het lichaam er uitzien en hoe ze moeten functioneren.
Maar soms treden er fouten in de celdeling op tot gevolg kunnen hebben dat er cellen met te veel kopieën van een chromosoom ontstaan of, omgekeerd, onvoldoende zijn. Er zijn twee soorten chromosoomafwijkingen:
- Numerieke, er zijn extra of ontbrekende chromosomen;
- Structurele, een chromosoom ontbreekt of ontbreekt een deel, het zit in een ander chromosoom of is omgekeerd.
Afwijkingen in het aantal en de opstelling van de chromosomen van het embryo zijn de meest voorkomende oorzaak van implantatie falen en vroege miskramen waarvan de kansen tevens verhogen in verband met de leeftijd van de moeder. Daarom is de PGT-A van aneuploïden een zeer nuttig instrument voor zowel de diagnose als de behandeling in onze Afdeling embryonale implantatie falen.
Andere keren treedt de afwijking op in een specifiek gen dat invloed heeft op de werking van het organisme en een monogenische aandoening veroorzaakt. Deze groep van aandoeningen kan op het nageslacht worden overgedragen.
Soorten Preïmplantatie Genetische Diagnostiek
- PGT-A chromosoomafwijkingen. De Preïmplantatie Genetische Test detecteert aneuploïden.
- PGT-M monogenische. De Preïmplantatie Genetische Test om monogenische aandoeningen te detecteren.
- PGT-SR diagnosticeert structurele afwijkingen.
Ze worden hieronder beschreven:
1. PGT-A de Preïmplantatie Genetische Test voor de analyse van aneuploïden (chromosoomafwijkingen)
| Chromosomale afwijkingen in embryo’s zijn één van de meest voorkomende oorzaken van een laag zwangerschapspercentage. Alleen embryo’s met een exact aantal chromosomen maken de geboorte van een gezonde baby mogelijk. Deze techniek maakt het mogelijk om de vervormde embryo’s uit te sluiten, ook al zijn ze door hun uiterlijk van goede kwaliteit.
Door het embryo niet terug te plaatsen vermijden wij dat het stel geconfronteerd wordt met de zwangerschap van een aangetaste baby, dat het embryo zich niet inplant of dat er een vroege miskraam plaatsvindt. Een extra kopie op chromosoom 21 zou bijvoorbeeld de oorzaak zijn van het ontstaan van het syndroom van Down (trisomie 21). Andere veel voorkomende chromosomale aneuploïden (één chromosoom te veel of te weinig) zijn trisomie 18, trisomie 15 of 47 en XXY (syndroom van Klinefelter). |
Aan wie wordt PGT-A aanbevolen?
- Als er sprake is van een hoge moederlijke leeftijd, ouder dan 35 jaar.
- Vrouwen die in twee of meer in-vitrofertilisatiecycli herhaalde miskramen en/of eerdere embryonale implantatie falen hebben gehad.
- Patiënten die chromosoomafwijkingen hebben gediagnosticeerd.
- Stellen waarbij is vastgesteld dat een ernstig mannelijk factor de oorzaak is van de vruchtbaarheidsproblemen.
Wat is de PGT-A stap voor stap
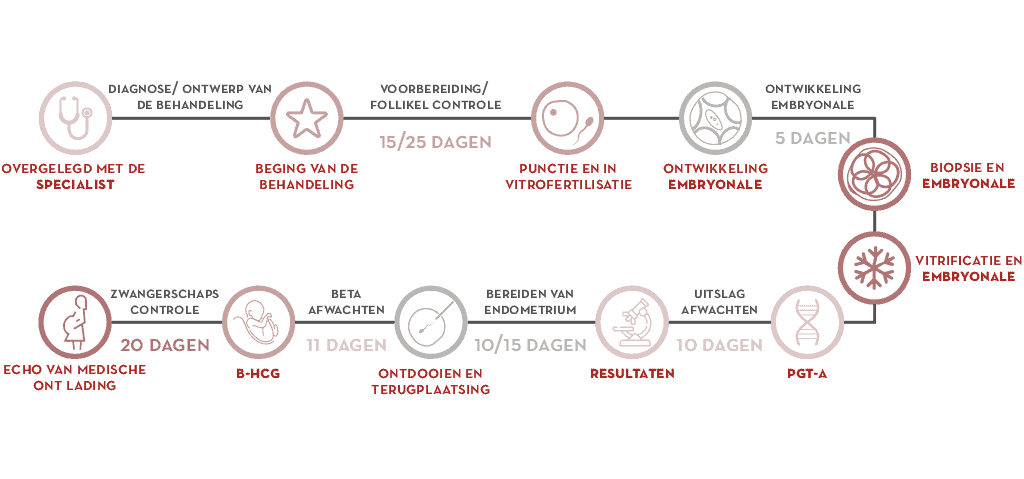
- De gynaecoloog zorgt tijdens het consult voor het ontwerp van de behandeling. Deze begint met de menstruatie.
- De ovariële stimulatie voor het verkrijgen van eicellen is de eerste stap.
- Na een in-vitro fertilisatiecyclus ontstaan de embryo’s.
- Wanneer het embryo 5-6 dagen oud is -blastocystfase – halen we een aantal cellen uit het embryo, via de embryobiopsietechniek.
- We cryopreserveren de embryo’s tot het moment van de terugplaatsing.
- De biopsie wordt verwerkt voor chromosoomanalyse. We krijgen de diagnose.
- Met uitslag bereiden we het endometrium van de moeder voor en de terugplaatsing van een embryo zonder chromosomale afwijkingen. De abnormale embryo’s sluiten we uit, zo voorkomen we onsuccesvolle terugplaatsingen.
2. PGT-M monogenische. De Preïmplantatie Genetische Test om monogenische ziekten te detecteren
| Het bestaat uit de genetische analyse van de embryo’s van een stel dat drager is van een erfelijke aandoening. Met deze test kan men de afwijking of mutatie in een gen opsporen die de aandoening veroorzaakt.
De eerste stap is het uitvoeren van een genetisch onderzoek van de toekomstige ouders om de fout in het gen (mutatie) te identificeren die de aandoening veroorzaakt -genetisch onderzoek -. Zodra we de uitslag van het genetische onderzoek hebben, is de volgende stap het uitvoeren van een informativiteitsonderzoek dat ons in staat stelt om een specifieke diagnostische strategie voor die aandoening in die familie te ontwerpen. De aandoeningen kunnen autosomaal recessief zijn, autosomaal-dominant, en chromosoom X-gebonden zoals Fragile X-syndroom, hemofilie A, cystische fibrose, de ziekte van Huntington, sikkelcelanemie, de ziekte van Marfan, enz. |
Aan wie wordt PGT-M aanbevolen?
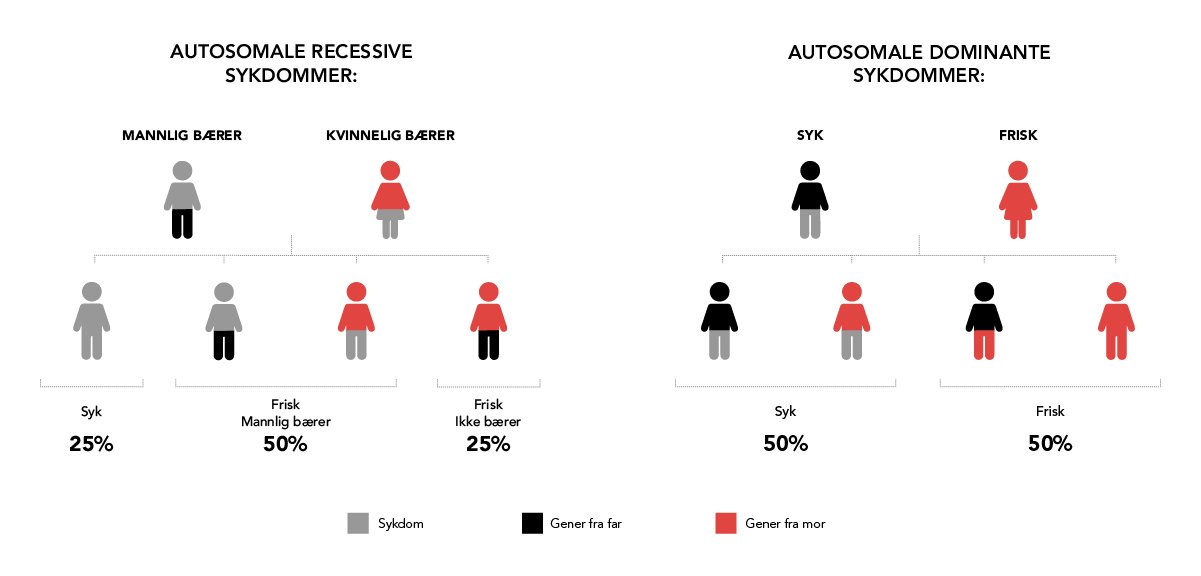
- Stellen waarbij één van de leden getroffen is door een genetische ziekte die overwegend erfelijk zou zijn (50% van hun kinderen zou ziek zijn).
- Stellen waarbij de moeder drager is van een geslachtsgebonden genetische ziekte (50% van haar kinderen zal ziek zijn).
- Stellen waarbij beide leden getroffen zijn door een genetische ziekte die overwegend erfelijk zou zijn (25% van hun kinderen zou ziek zijn).
Wat is de PGT-M stap voor stap
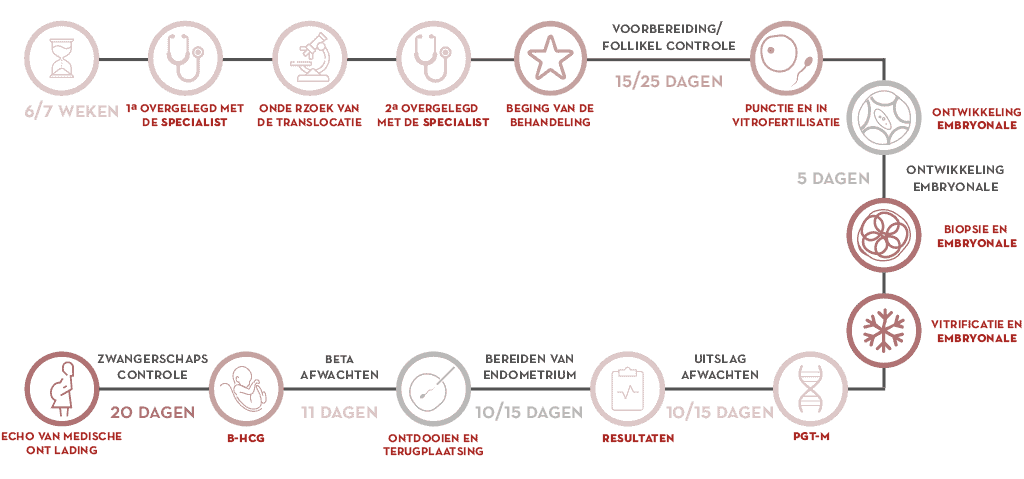
- De eerste stap is het genetisch onderzoek van de ouders. We moeten het specifieke geval aanpakken door de fout in het gen (mutatie) dat de aandoening veroorzaakt te identificeren.
- Vervolgens wordt het informativiteitsonderzoek uitgevoerd. Dit bestaat uit het ontwikkelen van de strategie die ons in staat stelt de afwijking in de embryo’s te identificeren. Het is vaak noodzakelijk voor gezonde en aangetaste familieleden om deel te nemen aan het onderzoek.
- De in-vitro fertilisatiecyclus begint. Zodra de vrouw ongesteld is, start de gecontroleerde ovariële stimulatie en tussen 15 en 25 dagen later worden de eicellen verkregen.
- In het laboratorium worden ze bevrucht met het sperma van de partner of de donor en worden ze gekweekt tot dag 5-6, een embryo in blastocystfase. Op dit moment voeren we de embryonale biopsie uit dat bestaat uit het extraheren van een aantal cellen voor genetische analyse. De embryo’s cryopreserveren we totdat we de uitslag hebben.
- De biopsie wordt verwerkt voor de genetische analyse. We krijgen de diagnose.
- Met de uitslag bereiden we het endometrium van de moeder voor en de terugplaatsing van het embryo zonder de afwijking in het bestudeerde gen.
3. PGT-SR de Preïmplantatie Genetische Test voor het opsporen van structurele afwijkingen
| Het detecteert embryo’s die abnormale chromosomen hebben omdat ze “gebroken” zijn of omdat er een verkeerde aanhechting van segmenten is. Deze structurele chromosoomafwijkingen zijn van vele aard: deleties, translocaties, doublures, inserties, inversies en ringen. De ziekte komt voor in gevallen waarin het gen niet correct tot uitdrukking kan komen door de afwijkende structuur van het chromosoom. |
Soorten structurele chromosoomafwijkingen
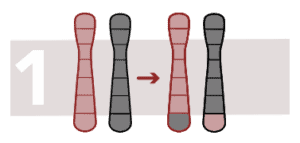
Evenwichtige wederzijdse translocatie
Een translocatie is een type chromosoomafwijking waarbij een chromosoom breekt en een stuk ervan zich vasthecht aan een ander chromosoom. Het is wederzijds wanneer het gebeurt door middel van segment-transfers tussen twee chromosomen, waardoor de configuratie verandert, maar niet het aantal chromosomen.
We spreken van een evenwichtige wederzijdse translocatie wanneer de opstelling geen verlies of winst van chromosomaal materiaal oplevert. Het komt voor wanneer een deel van een chromosoom van positie verandert in het genoom.
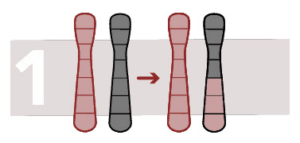
Onevenwichtige wederzijdse translocatie
De opstelling veroorzaakt een verlies of toename van chromosomaal materiaal. Er is een verandering in het aantal kopieën in een chromosomaal gebied. Het is mogelijk om fragmenten van een chromosoom te vinden in een ander chromosoom.
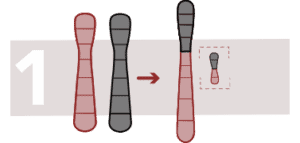
Robertsoniaanse Translocatie
Er vindt een fusie plaats tussen twee acrocentrische chromosomen (met slechts één arm), ze verliezen de uiteinden, de twee chromosomen voegen zich samen tot één. Men heeft dan 45 chromosomen in plaats van 46 en bestaat er een hoger risico voor trisomie.
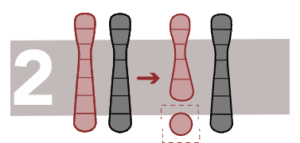
Deleties
Dit is het verlies van een fragment van DNA van een chromosoom.
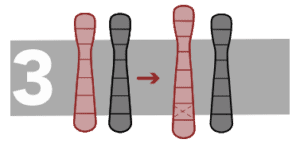
Duplicaties
Een segment van een chromosoom wordt na het originele fragment herhaald en produceert één of meer kopieën van een gen of een deel van een chromosoom.
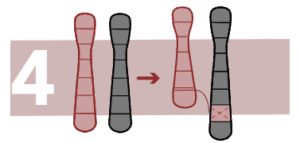
Inserties
Een deel van een chromosoom is ingebracht in een ongebruikelijke positie binnen hetzelfde of een ander chromosoom. Als er geen winst of verlies van chromosomaal materiaal is, zal de persoon gezond zijn.
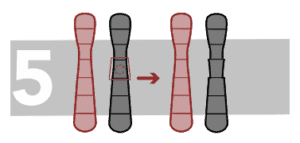
Paracentrische inversies
We hebben het over inversies wanneer een deel van het chromosoom in twee punten breekt en het binnenste segment ondersteboven draait en dan weer samenkomt. Paracentrische inversies komen voor wanneer de inversie niet de centromeer betreft.
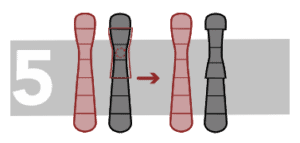
Pericentrische inversies
In dit geval omvat het omgekeerde fragment de centromeer.
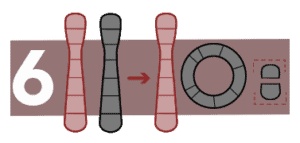
Ringen
De uiteinden van een chromosoom zijn afgebroken en aan de uiteinden samengevoegd tot een ring. Het veroorzaakt genetische aandoeningen, waarvan het syndroom van Turner de meest voorkomende is.
Aan wie wordt heet aanbevolen?
Aan stellen waarin één van de leden een drager is van een structurele chromosoomafwijking.
Wat is de PGT-SR stap voor stap
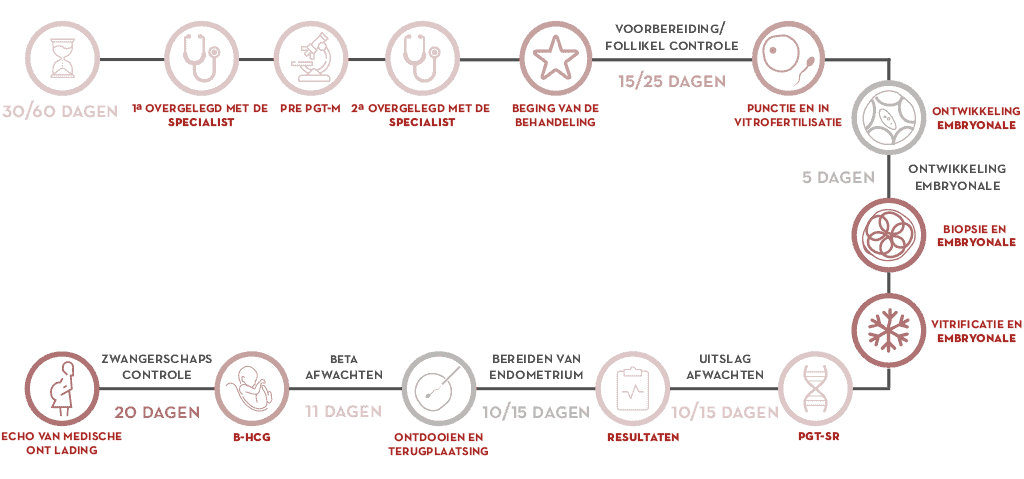
- Tijdens het eerste bezoekje beoordeelt de gynaecoloog het geval.
- Het kan zijn dat er een voorafgaand onderzoek van de structurele afwijking nodig is.
- In het volgende consult zal de diagnose en het ontwerp van de behandeling worden vastgesteld. De behandeling begint met de menstruatie.
- De ovariële stimulatie voor het verkrijgen van eicellen is de eerste stap.
- Na een in-vitro fertilisatiecyclus ontstaan de embryo’s.
- Wanneer het embryo 5-6 dagen oud is -blastocystfase – halen we een aantal cellen uit het embryo, via de embryobiopsietechniek.
- We cryopreserveren de embryo’s tot het moment van de terugplaatsing.
- De biopsie wordt verwerkt voor chromosoomanalyse. We krijgen de diagnose.
- Aan der hand van de uitslag bereiden we het endometrium van de moeder voor en de terugplaatsing van een gezond embryo, of met andere woorden, een embryo zonder chromosomale afwijkingen. Abnormale embryo’s worden uitgesloten, zo voorkomen we onsuccesvolle terugplaatsingen.
Voordelen van een PGD/PGT
Het bevordert de embryoselectie, we weten welke embryo’s het aantal chromosomen niet hebben veranderd en tot een gezond kind zal leiden.
Het voorkomt dat embryo’s die niet innestelen worden teruggeplaatst. Er zijn chromosomale afwijkingen die onverenigbaar zijn met het leven en die de ontwikkeling van het embryo in het beginstadium verhinderen of niet in de baarmoeder van de moeder kan innestelen.
Embryo’s die miskramen of geboorten van kinderen met verschillende syndromen veroorzaken, zullen niet innestelen.
Het verkort de tijd om een zwangerschap te bereiken. We voorkomen het terugplaatsen van embryo’s die niet leiden tot een gezond kind of die tijdens de ontwikkeling zullen blokkeren.
Lagere kosten. Het zal het invriezen en terugplaatsen van embryo’s die niet genetisch gezond zijn, zelfs als ze er zo uitzien, vermijden, waardoor de kosten voor het terugplaatsen van deze embryo’s, waarvan we weten dat ze niet levensvatbaar zijn, worden geëlimineerd.
Het verbetert het psychologisch welzijn. Het garandeert dat het embryo gezond is en verlaagt de kans op een miskraam en daarmee de emotionele stress die dit met zich meebrengt voor het stel.
Nadelen van PGD/PGT
Het is een invasieve procedure omdat het embryo moet worden gebiopteerd om de genetische test uit te voeren.
Cyclus zonder terugplaatsing Het risico bestaat dat alle embryo’s chromosomaal abnormaal zijn en dat er geen terugplaatsing kan plaatsvinden. Dit leidt enerzijds tot een onderbreking van de behandeling en anderzijds tot een emotionele tegenslag.
Embryonale mozaïek. Dankzij de nauwkeurigheid van de genetische analysetechnieken kunnen we weten of het embryo normale en afwijkende cellen heeft, bekend als mozaïek. Of dit het embryo op enigerlei wijze beïnvloedt, moet nog worden vastgesteld. Verschillende onderzoeken van Instituto Bernabeu gaan in deze richting.
Screeningmethode De biopsie van het embryo analyseert het uitwendige deel om het deel dat de baby zal voortbrengen intact te laten. Tal van wetenschappelijke documenten hebben een hoge mate van correlatie tussen beide. We gaan ervan uit dat het monster dat we nemen representatief is voor het hele embryo.
Moeilijkheid om de beslissing te nemen. Veel stellen vinden het pijnlijk om de beslissing te nemen om hun embryo’s te testen, hetzij vanwege ethische of emotionele kwesties. Daarnaast krijgen ze in ons centrum, genetisch, psychologisch en professioneel advies om hen desgewenst te begeleiden.